- 薬事関係法規・制度
- 3.医薬品の分類・取扱い等
- 医薬品の分類・取扱い等
- Sec.1
1医薬品の分類・取扱い等
■医薬品の定義と範囲ー1
医薬品の定義は、法第2条第1項において次のように規定されている。
「一 日本薬局方に収められている物
二 人又は動物の疾病の診断、治療又は予防に使用されることが目的とされている物であつて、機械器具等(機械器具、歯科材料、医療用品、衛生用品並びにプログラム(電子計算機に対する指令であつて、一の結果を得ることができるように組み合わされたものをいう。以下同じ。)及びこれを記録した記録媒体をいう。以下同じ。)でないもの(医薬部外品及び再生医療等製品を除く。)
三 人又は動物の身体の構造又は機能に影響を及ぼすことが目的とされている物であつて、機械器具等でないもの(医薬部外品及び化粧品を除く。)」
第1号に規定されている日本薬局方(以下「日局」という。)とは、法第41条第1項の規定に基づいて、厚生労働大臣が医薬品の性状及び品質の適正を図るため、薬事・食品衛生審議会の意見を聴いて、保健医療上重要な医薬品(有効性及び安全性に優れ、医療上の必要性が高く、国内外で広く使用されているもの)について、必要な規格・基準及び標準的試験法等を定めたものである。日局に収載されている医薬品の中には、一般用医薬品として販売されている、又は一般用医薬品の中に配合されているものも少なくない。
第2号に規定されている医薬品は、疾病の診断、治療又は予防に使用されることを目的とするものであり、社会通念上いわゆる医薬品と認識される物の多くがこれに該当する。これには検査薬や殺虫剤、器具用消毒薬のように、人の身体に直接使用されない医薬品も含まれる。
第3号に規定されている医薬品は、人の身体の構造又は機能に影響を及ぼすことが目的とされている物のうち、第1号及び第2号に規定されているもの以外のものが含まれる。これに該当するものとしては、「やせ薬」を標榜(ぼう)したもの等、「無承認無許可医薬品」が含まれる。
医薬品は、厚生労働大臣により「製造業」の許可を受けた者でなければ製造をしてはならないとされており(法第13条第1項)、厚生労働大臣により「製造販売業」の許可を受けた者でなければ製造販売をしてはならないとされている(法第12条第1項)。また、その医薬品は、品目ごとに、品質、有効性及び安全性について審査等を受け、その製造販売について厚生労働大臣の承認を受けたものでなければならないとされている(法第14条又は法第19条の2)。必要な承認を受けずに製造販売された医薬品の販売等は禁止されており(法第55条第2項)、これらの規定に違反して販売等を行った者については、「三年以下の懲役若しくは三百万円以下の罰金に処し、又はこれを併科する」(法第84条第2号、第3号、18号)こととされている。
必要な承認等を受けていない医薬品の広告の禁止に関する出題については、本章Ⅳ-1)(適正な販売広告)を参照のこと。
また、製造販売元の製薬企業、製造業者のみならず、薬局及び医薬品の販売業においても、不正表示医薬品(法第50から54条違反)及び次に掲げる不良医薬品は、販売し、授与し、又は販売若しくは授与の目的で製造し、輸入し、貯蔵し、若しくは陳列してはならないとされている(法第55条、第56条)。
(a) 日本薬局方に収められている医薬品であって、その性状、品質が日本薬局方で定める基準に適合しないもの
(b) 法第14条、法第19条の2、法第23条の2の5又は法第23条の2の17の承認を受けた医薬品であって、その成分若しくは分量又は性状、品質若しくは性能がその承認の内容と異なるもの
(c) 法第14条第1項、法第23条の2の5第1項又は第23条の2の23第1項の規定により厚生労働大臣が基準を定めて指定した医薬品であって、その成分若しくは分量又は性状又は品質若しくは性能がその基準に適合しないもの
(d) 法第42条第1項の規定によりその基準が定められた医薬品であって、その基準に適合しないもの
(e) その全部又は一部が不潔な物質又は変質若しくは変敗した物質から成っている医薬品
(f) 異物が混入し、又は付着しているもの
(g) 病原微生物その他疾病の原因となるものにより汚染され、又は汚染されているおそれがあるもの
(h) 着色のみを目的として、厚生労働省令で定めるタール色素以外のタール色素が使用されている医薬品
また同様に、次に該当する医薬品も、販売し、授与し、又は販売若しくは授与の目的で製造し、輸入し、若しくは陳列してはならないとされている(法第57条)。
(a) 医薬品は、その全部若しくは一部が有毒若しくは有害な物質からなっているためにその医薬品を保健衛生上危険なものにするおそれがある物とともに収められていてはならない
(b) 医薬品は、その全部若しくは一部が有毒若しくは有害な物質からなっているためにその医薬品を保健衛生上危険なものにするおそれがある容器若しくは被包(内包を含む。)に収められていてはならない
(c) 医薬品の容器又は被包は、その医薬品の使用方法を誤らせやすいものであってはならない
これらの規定に触れる医薬品(不良医薬品)の製造、輸入、販売等を行った者については、「三年以下の懲役若しくは三百万円以下の罰金に処し、又はこれを併科する」(法第84条第18号から第20号)こととされている。
また、これらの規定については、製造販売元の製薬企業、製造業者のみならず、薬局及び医薬品の販売業においても適用されるものであり、販売又は授与のため陳列がなされる際に適正な品質が保たれるよう十分留意される必要がある。
■医薬品の定義と範囲ー2
【一般用医薬品、要指導医薬品と医療用医薬品】
一般用医薬品は、法第4条第5項第4号において次のように規定されている。
「医薬品のうち、その効能及び効果において人体に対する作用が著しくないものであつて、薬剤師その他の医薬関係者から提供された情報に基づく需要者の選択により使用されることが目的とされているもの(要指導医薬品を除く。)」
|
|
要指導医薬品及び一般用医薬品 |
|
|||||
|
|
リスク区分 |
|
対応する専門家 |
|
販売者から |
|
|
|
|
要指導医薬品 |
|
薬剤師 |
|
対面で書面での情報提供及び薬学的知見に基づく指導(義務) |
|
|
|
|
一般用医薬品 |
第一類医薬品 |
|
薬剤師 |
|
書面での情報提供(義務) |
|
|
|
第二類医薬品 |
|
薬剤師または |
|
努力義務 |
|
|
|
|
第三類医薬品 |
|
薬剤師または |
|
法律上の規定なし |
|
|
|
|
|
|
|
|
|
|
|
また、要指導医薬品は、法第4条第5項第3号において次のように規定されている。
「次のイからニまでに掲げる医薬品(専ら動物のために使用されることが目的とされているものを除く。)のうち、その効能及び効果において人体に対する作用が著しくないものであつて、薬剤師その他の医薬関係者から提供された情報に基づく需要者の選択により使用されることが目的とされるものであり、かつ、その適正な使用のために薬剤師の対面による情報の提供及び薬学的知見に基づく指導が行われることが必要なものとして、厚生労働大臣が薬事・食品衛生審議会の意見を聴いて指定するものをいう。
イ その製造販売の承認の申請に際して第14条第8項に該当するとされた医薬品であつて、当該申請に係る承認を受けてから厚生労働省令で定める期間を経過しないもの
ロ その製造販売の承認の申請に際してイに掲げる医薬品と有効成分、分量、用法、用量、効能、効果等が同一性を有すると認められた医薬品であつて、当該申請に係る承認を受けてから厚生労働省令で定める期間を経過しないもの
ハ 第44条第1項に規定する毒薬
ニ 第44条第2項に規定する劇薬」
医薬品には、一般用医薬品、要指導医薬品のほか、医師若しくは歯科医師によって使用され、又はこれらの者の処方箋若しくは指示によって使用されることを目的として供給されるもの(医療用医薬品)がある。医療用医薬品は、「医師若しくは歯科医師によって使用され又はこれらの者の処方箋若しくは指示によって使用されることを目的として供給される医薬品」であり、一般用医薬品及び要指導医薬品は、「薬剤師その他の医薬関係者から提供された情報に基づく需要者の選択により使用されることが目的とされているもの」である。そのため、一般用医薬品又は要指導医薬品では、注射等の侵襲性の高い使用方法は用いられておらず、人体に直接使用されない検査薬においても、検体の採取に身体への直接のリスクを伴うもの(例えば、血液を検体とするもの)は、一般用医薬品又は要指導医薬品としては認められていない。
用量に関しては、医療用医薬品は、医師又は歯科医師が診察をして患者の容態に合わせて処方量を決めて交付するものであり、一般用医薬品及び要指導医薬品は、あらかじめ定められた用量に基づき、適正使用することによって効果を期待するものである。
|
|
一般用医薬品及び医療用医薬品 |
|
||||
|
|
|
|
一般用医薬品 |
|
医療用医薬品 |
|
|
|
定義 |
|
一般の人が薬局等で購入し、自らの判断で使用する医薬品。安全性が確保できる成分の配合によるものが多い。 |
|
医師(歯科医師)によって使用され又はこれらの者の処方せん又は指示によって使用されることを目的として供給される医薬品 |
|
|
|
効能・効果 |
|
一般の人が自ら判断できる症状 |
|
医師の診断疾患名 |
|
|
|
用法・用量 |
|
一般の人が自らの判断で適用できるよう、 ・一般の人が使いやすい剤型 ・用量はあらかじめ定められている |
|
医師が自ら又はその指導監督下で使用するため、用法や剤型に特に制限はない |
|
|
|
使用上の |
|
一般の人に理解しやすいもの |
|
医師、薬剤師等の医療関係者にとって見やすくわかりやすいもの |
|
|
|
|
|
|
|
|
|
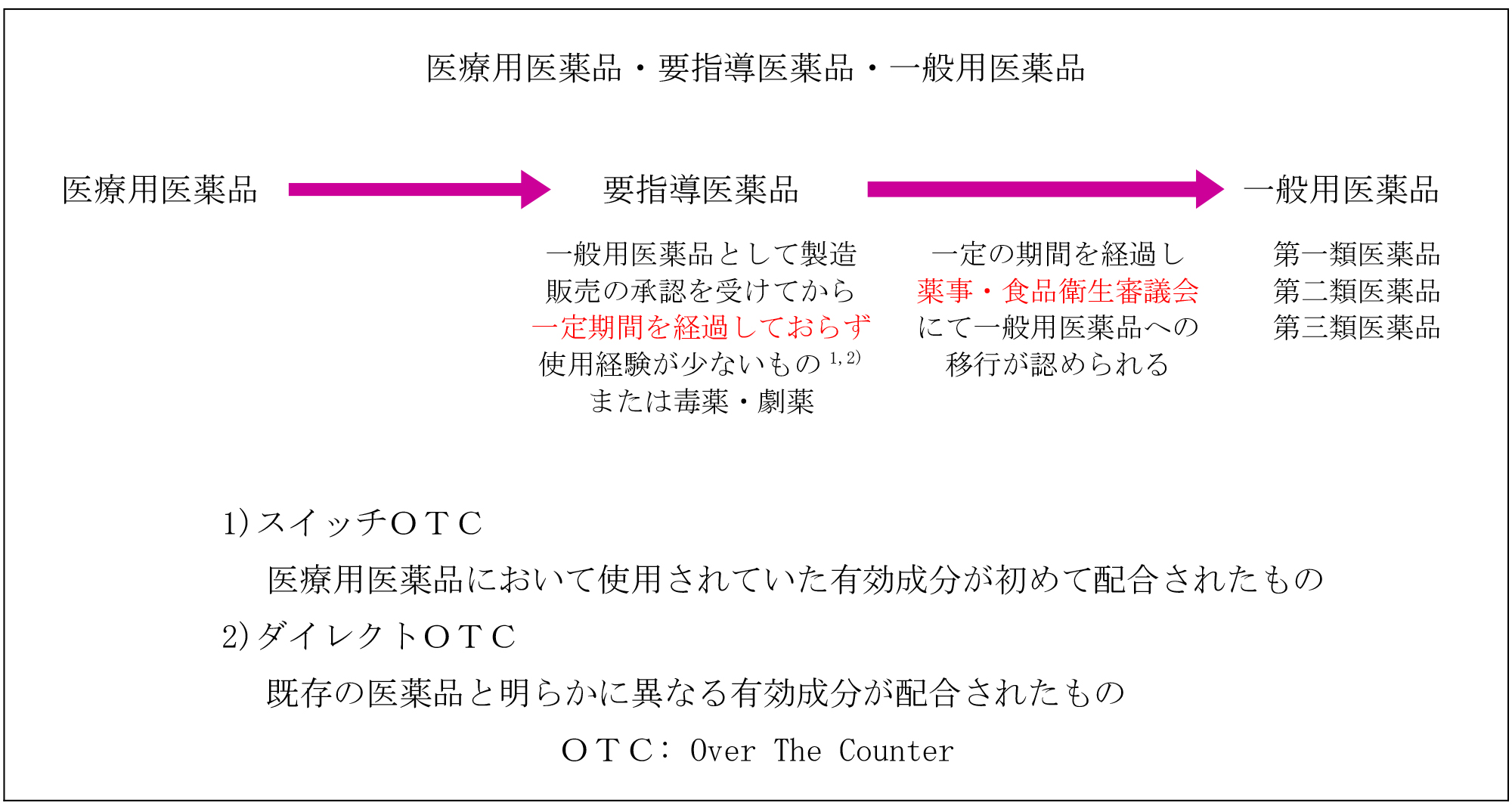
効能効果の表現に関しては、医療用医薬品では通常、診断疾患名(例えば、胃炎、胃・十二指腸潰瘍等)で示されているのに対し、一般用医薬品及び要指導医薬品では、一般の生活者が判断できる症状(例えば、胃痛、胸やけ、むかつき、もたれ等)で示されている。なお、一般用医薬品及び要指導医薬品は、通常、医療機関を受診するほどではない体調の不調や疾病の初期段階において使用されるものであり、医師等の診療によらなければ一般に治癒が期待できない疾患(例えば、がん、心臓病等)に対する効能効果は、一般用医薬品及び要指導医薬品において認められていない。
薬剤師その他医薬関係者から提供された情報に基づく需要者の選択により使用されることを目的とする医薬品であって、医療用医薬品において使用されていた有効成分が初めて配合されたものや既存の医薬品と明らかに異なる有効成分が配合されたもののうち、その適正な使用のために薬剤師の対面による情報の提供及び薬学的知見に基づく指導が行われることが必要なものについては、薬事・食品衛生審議会の意見を聴いた上で、厚生労働大臣が要指導医薬品として指定する。要指導医薬品は、次に掲げる期間を経過し、薬事・食品衛生審議会において、一般用医薬品として取り扱うことが適切であると認められたものについては、一般用医薬品に分類される。
(a) 法第4条第5項第3号イに該当する要指導医薬品(規則第7条の2第1項)
① 法第14条の4第1項第1号に規定する新医薬品:法第14条の4第1項第1号に規定する調査期間(同条第2項の規定による延長が行われたときは、その延長後の期間)
|
新医薬品
既に(略)承認を与えられている医薬品と有効成分、分量、用法、用量、効能、効果等が明らかに異なる医薬品として厚生労働大臣がその承認の際指示したもの (薬機法第14条の4第1項第1号) |
② 法第79条第1項の規定に基づき、製造販売の承認の条件として当該承認を受けた者に対し製造販売後の安全性に関する調査を実施する義務が課せられている医薬品:製造販売の承認の条件として付された調査期間
(b) 法第4条第5項第3号ロに該当する要指導医薬品(規則第7条の2第2項)
当該要指導医薬品と有効成分、分量、用法、用量、効能、効果等が同一性を有すると認められた(a)の要指導医薬品に係る①又は②の期間の満了日までの期間
また、販売における規制の違いとして、店舗販売業は、一般用医薬品及び要指導医薬品以外の医薬品の販売等は認められておらず(法第27条)、配置販売業は一般用医薬品(経年変化が起こりにくいことその他の厚生労働大臣の定める基準に適合するものに限る。)以外の医薬品の販売は認められていない(法第31条)。したがって、医療用医薬品の販売は、薬局及び卸売販売業者に限られる。
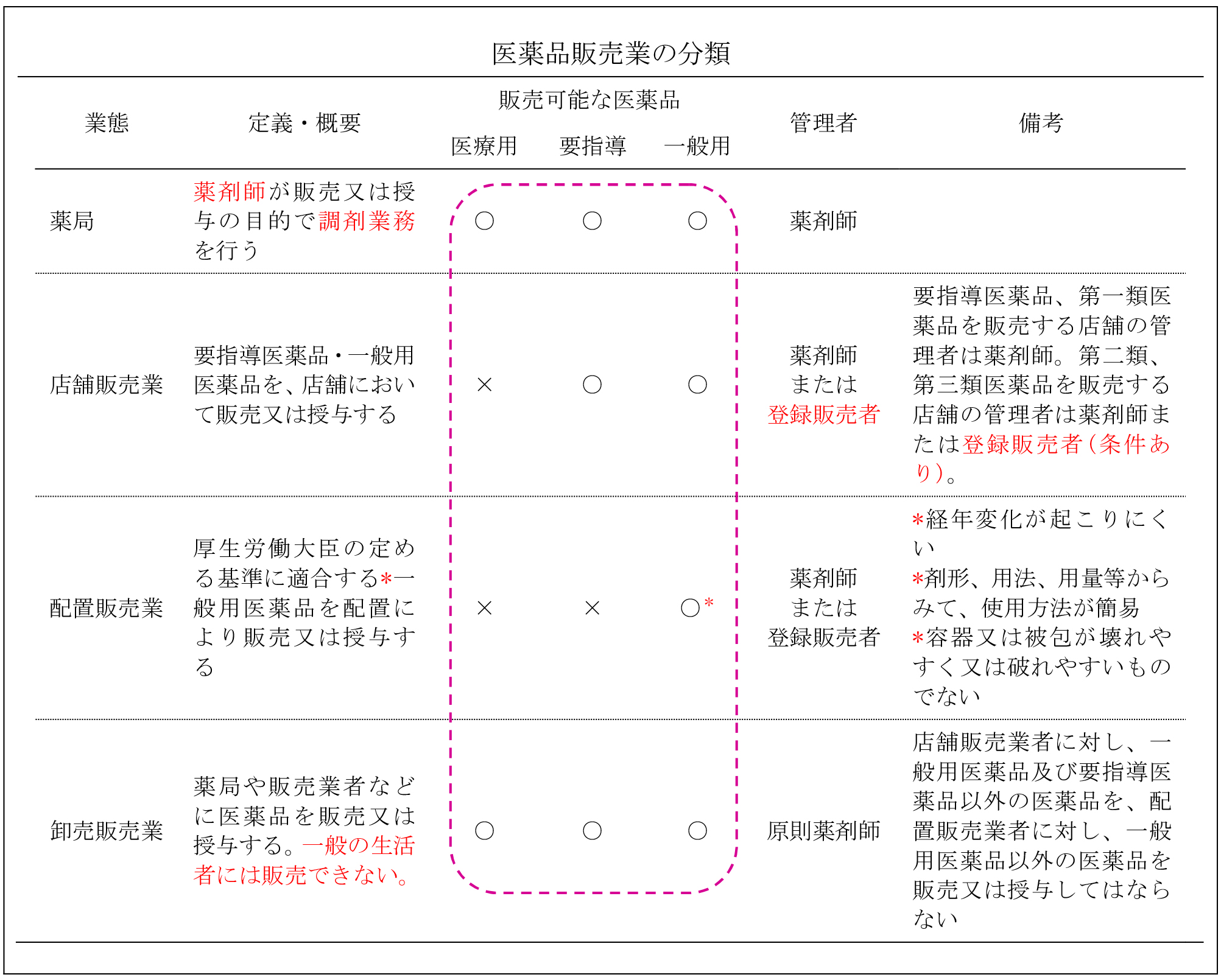
卸売販売業者は、店舗販売業者に対し、一般用医薬品及び要指導医薬品以外の医薬品を、配置販売業者に対し、一般用医薬品以外の医薬品を販売又は授与してはならないこととなっている。(規則第158条の2)
■医薬品の定義と範囲ー3
【毒薬・劇薬】
毒薬とは、法第44条第1項の規定に基づき、毒性が強いものとして厚生労働大臣が薬事・食品衛生審議会の意見を聴いて指定する医薬品をいう。また、劇薬とは、同条第2項の規定に基づき、劇性が強いものとして厚生労働大臣が薬事・食品衛生審議会の意見を聴いて指定する医薬品をいう。
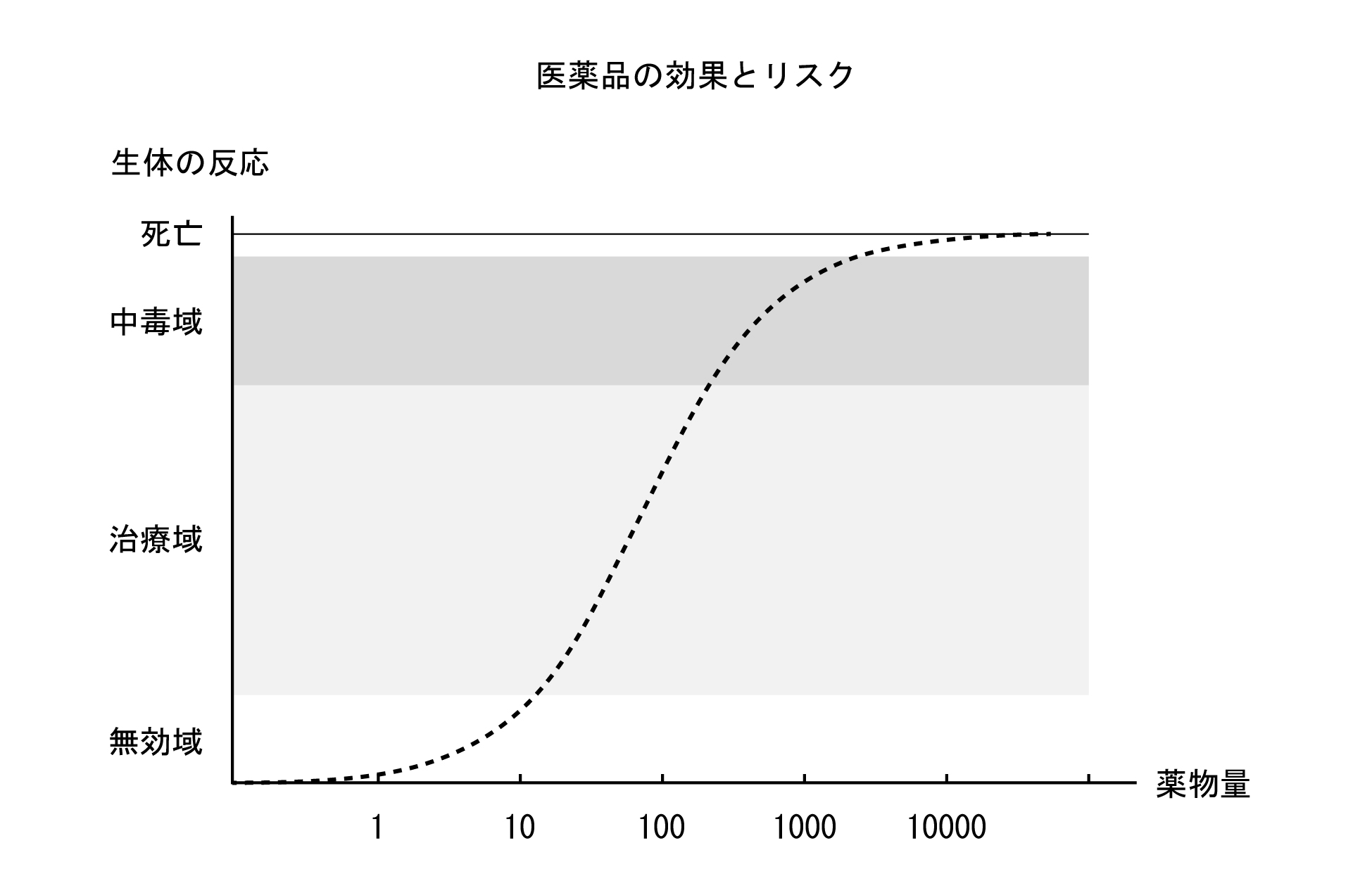
毒薬及び劇薬は、単に毒性、劇性が強いものだけでなく、薬効が期待される摂取量(薬用量)と中毒のおそれがある摂取量(中毒量)が接近しており安全域が狭いため、その取扱いに注意を要するもの等が指定され、販売は元より、貯蔵及びその取り扱いは、他の医薬品と区別されている。なお、一般用医薬品で毒薬又は劇薬に該当するものはなく、要指導医薬品で毒薬又は劇薬に該当するものは一部に限られている。

業務上毒薬又は劇薬を取り扱う者(薬局開設者又は医薬品の販売業の許可を受けた事業者(以下「医薬品の販売業者」という。)を含む。)は、それらを他の物と区別して貯蔵、陳列しなければならず、特に毒薬を貯蔵、陳列する場所については、かぎを施さなければならないとされている(法第48条第1項及び第2項)。これに違反した者については、「一年以下の懲役若しくは百万円以下の罰金に処し、又はこれを併科する」(法第86条第1項第12号)こととされている。
毒薬については、それを収める直接の容器又は被包(以下「容器等」という。)に、黒地に白枠、白字をもって、当該医薬品の品名及び「毒」の文字が記載されていなければならず、劇薬については、容器等に白地に赤枠、赤字をもって、当該医薬品の品名及び「劇」の文字が記載されていなければならないとされている(法第44条第1項及び第2項)。
この規定に触れる毒薬又は劇薬は、販売等してはならないとされており(法第44条第3項)、これに違反した者については、「三年以下の懲役若しくは三百万円以下の罰金に処し、又はこれを併科する」こととされている(法第84条第16号)。このほか、法定表示事項に共通する規定に関する出題については、Ⅱ-2)(容器・外箱等への記載事項、添付文書等への記載事項)を参照して作成のこと。
また、毒薬又は劇薬を、14歳未満の者その他安全な取扱いに不安のある者に交付することは禁止されており(法第47条)、これに違反した者については、「二年以下の懲役若しくは二百万円以下の罰金に処し、又はこれを併科する」(法第85条第2号)こととされている。この場合、「安全な取扱いに不安がある者」とは、「睡眠薬の乱用」「不当使用」等が懸念される購入希望者等をさす。
さらに、毒薬又は劇薬を、一般の生活者に対して販売又は譲渡する際には、当該医薬品を譲り受ける者から、品名、数量、使用目的、譲渡年月日、譲受人の氏名、住所及び職業が記入され、署名又は記名押印された文書の交付を受けなければならない(法第46条第1項及び規則第205条)。また、毒薬又は劇薬については、店舗管理者が薬剤師である店舗販売業者及び営業所管理者が薬剤師である卸売販売業者以外の医薬品の販売業者は、開封して、販売等してはならないとされている(法第45条)。これらの規定に違反して販売等した者については、「一年以下の懲役若しくは百万円以下の罰金に処し、又はこれを併科する」(法第86条第1項第10号又は第11号)こととされている。